| Amidas |
Síntesis
- A partir de haluros de ácido
- A partir de anhidridos
- A partir de ésteres
- A partir de ácidos carboxílicos:


| Nitrilos |
Síntesis

- Obtención de ácidos carboxílicos mediante hidrólisis de nitrilos
- Reducción:


| Haluros de ácido |


| Anhidridos |


| Esteres |







| Acidos carboxílicos |


 |
| ACIDO CARBOXILICO |
| Estructura | Nombre IUPAC | Nombre común | Fuente natural |
|---|---|---|---|
| HCOOH | Ácido metanoico | Ácido fórmico | Destilación destructiva de hormigas (formica en latín) |
| CH3COOH | Ácido etanoico | Ácido acético | Fermentación del vino (vinagre) |
| CH3CH2COOH | Ácido propanoico | Ácido propiónico | Fermentación de lácteos (pion en griego) |
| CH3CH2CH2COOH | Ácido butanoico | Ácido butírico | Mantequilla (butyrum, en latín) |
| CH3(CH2)3COOH | Ácido pentanoico | Ácido valérico | Raíz de la valeriana officinalis |
| CH3(CH2)4COOH | Ácido hexanoico | Ácido caproico | grasa de cabra |
| FORMULA | NOMBRE IUPAC | NOMBRE TRIVIAL |
|---|---|---|
| HOOC-COOH | Ac. Etanodioico | Ac. Oxálico |
| HOOC-CH2-COOH | Ac. Propanodioico | Ac. Malónico |
| HOOC-(CH2)2-COOH | Ac. Butanodioico | Ac. Succínico |













| Localizador | Cadena Carbonada Principal | Carbaldehido | Ejemplo |
|---|---|---|---|
| 1(se puede omitir) | Benceno | Carbaldehido | |
| 2,3 | Naftaleno | DiCarbaldehido |
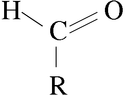 Es decir, el grupo carbonilo H-C=O está unido a un solo radical orgánico.
Es decir, el grupo carbonilo H-C=O está unido a un solo radical orgánico.| Número de carbonos | Nomenclatura IUPAC | Nomenclatura trivial | Fórmula | P.E.°C |
|---|---|---|---|---|
| 1 | Metanal | Formaldehído | HCHO | -21 |
| 2 | Etanal | Acetaldehído | CH3CHO | 20,2 |
| 3 | Propanal | Propionaldehído Propilaldehído | C2H5CHO | 48,8 |
| 4 | Butanal | n-Butiraldehído | C3H7CHO | 75,7 |
| 5 | Pentanal | n-Valeraldehído Amilaldehído n-Pentaldehído | C4H9CHO | 103 |
| 6 | Hexanal | Capronaldehído n-Hexaldehído | C5H11CHO | |
| 7 | Heptanal | Enantaldehído Heptilaldehído n-Heptaldehído | C6H13CHO | |
| 8 | Octanal | Caprilaldehído n-Octilaldehído | C7H15CHO | |
| 9 | Nonanal | Pelargonaldehído n-Nonilaldehído | C8H17CHO | |
| 10 | Decanal | Caprinaldehído n-Decilaldehído |

| etanol |
| Tipo | Reacción | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hidrogenación |
| |||||||||||
| Hidro- halogenación (X = Cl, Br, I) (markovnikov) |
| |||||||||||
| Hidro- bromación con peróxidos (antimarkovnikov) |
| |||||||||||
| Hidratación (markovnikov) |
| |||||||||||
| Hidroboración- oxidación (antimarkovnikov) |
| |||||||||||
| Halogenación (X = Cl, Br) |
| |||||||||||
| Ozonólisis |
| |||||||||||
| Tratamiento con KMnO4 en caliente |
| |||||||||||
| Acidez de alquinos terminales |
|